
Die Pharmaindustrie ist über eine Billion Dollar wert und hatte traditionell eine konservative Perspektive. KI bietet großes Potenzial, die Pharmaindustrie zu verändern, in allen Geschäftsphasen enorme Kosteneinsparungen zu erzielen und mit Anwendungsfällen wie der Kostenmodellierung für klinische Studien mit NLP die Finanzplanung zu beeinflussen. Wie KI im Gesundheitswesen im Allgemeinen hat auch die Nutzung von maschinellem Lernen , natürlicher Sprachverarbeitung und KI in der Pharmaindustrie gerade erst begonnen, und Pharmaunternehmen erzielen bereits große Renditen auf ihre Anfangsinvestitionen . Bei Fast Data Science sind wir auf die Anwendung von natürlicher Sprachverarbeitung und KI auf Probleme in der Pharma- und Gesundheitsbranche spezialisiert. Um mehr zu erfahren, lesen Sie weiter oder setzen Sie sich mit uns in Verbindung .
Thomas Wood demonstriert das Clinical Trial Risk Tool , eine Anwendung von NLP und KI in der Pharmaindustrie .
Die erste Phase der Arzneimittelentwicklung ist die Arzneimittelentdeckungsphase , in der Kandidatenverbindungen entdeckt werden, bevor sie an Menschen getestet werden. In der Vergangenheit wurden Kandidatenmedikamente entdeckt, indem der Wirkstoff in traditionellen Heilmitteln identifiziert wurde. Im 19. Jahrhundert beispielsweise isolierten Chemiker Salicylsäure aus der Rinde der Weide, die lange als Volksheilmittel zur Behandlung von Kopfschmerzen verwendet wurde, und daraus entstand die Grundlage für Aspirin, das heute weit verbreitet ist.

Heutzutage umfasst die Arzneimittelforschung das Screening von Millionen von Molekülen . Dabei werden zunächst hochentwickelte Computerprogramme verwendet, um die Wechselwirkung der Moleküle mit Zielmolekülen im menschlichen Körper zu simulieren. Dieser Prozess wird in silico genannt, eine neulateinische Analogie zu in vivo – an lebenden Versuchspersonen – und in vitro – in Reagenzgläsern und Petrischalen.
Vor der explosionsartigen Zunahme von KI-Anwendungsfällen in der Pharmaindustrie simulierten Forscher Molekülinteraktionen mithilfe von Software, die mit den Gesetzen der Physik und Chemie vorprogrammiert war. In jüngster Zeit gibt es einen Trend, maschinelles Lernen in der Pharmaindustrie einzusetzen, um herauszufinden, welche Art von Proteinen mit welchen Zielen interagieren, und um die Ergebnisse auf neue, noch nicht bekannte Moleküle zu übertragen, die noch nicht synthetisiert wurden.
Ein besonders schwieriges Problem ist die Vorhersage, wie sich eine Aminosäuresequenz zu einer dreidimensionalen Struktur (einem Protein) faltet. 2016 entwickelten Forscher bei DeepMind AlphaFold, das dreidimensionale Formen aus Datenbanken bekannter Proteine „lernen“ und die Form einer neuen Sequenz vorhersagen kann. Das in Utah ansässige KI-/Pharmaunternehmen Recursion Pharmaceuticals übernimmt die Vorhersagen von AlphaFold und testet sie experimentell.
2015 entwickelte das in San Francisco ansässige Startup Atomwise einen Algorithmus namens AtomNet, der auf einem Convolutional Neural Network (CNN) basiert. Dieser Algorithmus basierte auf einem Datensatz beobachteter Wechselwirkungen zwischen Molekülen und war in der Lage, einige Regeln der organischen Chemie zu erlernen, ohne dass man ihm diese explizit beibringen musste. Atomwise nutzte AtomNet, um Spitzenkandidaten für Arzneimittelforschungsprogramme zu identifizieren. So fand das Unternehmen beispielsweise einen Kandidaten im Kampf gegen das Ebola-Virus, der später in vorklinische Tests überging.
 [algorithms](https://harmonydata.ac.uk/measuring-the-performance-of-nlp-algorithms). Image source: Segura-Bedmar et al (2014)](https://fastdatascience.com/images/ddi-min.jpg)
AI in pharma
Einige kommentierte Texte im DDI-Korpus, die bei der DDIExtraction Challenge verwendet wurden, zeigen markierte Arzneimittelinteraktionen, die zum Trainieren von maschinellen Lernalgorithmen in der Pharmaindustrie verwendet werden können. Bildquelle: Segura-Bedmar et al (2014)
Bei Fast Data Science haben wir an einem Projekt für Boehringer Ingelheim gearbeitet, bei dem das Unternehmen eine Reihe proprietärer Moleküle als Open Source zur Verfügung gestellt hat. Forscher können kostenlos Proben der betreffenden Verbindungen bestellen, und die Molekülstruktur wird online und in der Literatur veröffentlicht.
Das Unternehmen war daran interessiert, Veröffentlichungen zu verfolgen, in denen die Autoren Moleküle von Boehringer verwendeten, unabhängig davon, ob Boehringer zitiert wurde oder nicht, um neue Entwicklungen zu verfolgen, die sich aus den Entdeckungen ergeben, und potenzielle zukünftige Kooperationen zu identifizieren. Fast Data Science entwickelte einen maßgeschneiderten Algorithmus zur Verarbeitung natürlicher Sprache, um Kooperationen und Erwähnungen von Molekülen zu verfolgen und sie dem Arzneimittelforschungsteam zu melden, selbst wenn eine Variante des Molekülnamens verwendet wird.
| Pharma company | 2022 revenue |
|---|---|
| Pfizer | $100.33 billion |
| Johnson & Johnson | $94.94 billion |
| Roche | $66.26 billion |
| Merck & Co. | $59.28 billion |
| AbbVie | $58.05 billion |
| Novartis | $50.54 billion |
| Bristol Myers Squibb | $46.16 billion |
| Sanofi | $45.22 billion |
| AstraZeneca | $44.35 billion |
| GSK | $36.15 billion |
| Takeda | $30.00 billion |
| Eli Lilly | $28.55 billion |
| Gilead Sciences | $27.28 billion |
| Bayer | $26.64 billion |
| Amgen | $26.32 billion |
| Boehringer Ingelheim | $25.28 billion |
| Novo Nordisk | $25.00 billion |
| Moderna | $18.47 billion |
| Merck KGaA | $19.16 billion |
| BioNTech | $18.20 billion |
Top-Pharmaunternehmen weltweit nach Umsatz im Jahr 2022. Datenquelle
Um wettbewerbsfähig zu bleiben, investieren Pharmaunternehmen enorme Summen in Marktforschungsaktivitäten. Sie befragen beispielsweise Ärzte zur Verwendung und Verschreibung bestehender Medikamente oder durchforsten Krankenakten und Berichte nach Beschreibungen unerwünschter Ereignisse (UE), selbst bei Medikamenten, die bereits die vierte Phase der klinischen Tests durchlaufen und die Zulassung der FDA erhalten haben.
In der Pharmaindustrie gibt es viele kleinere Akteure, die Marktforschung, Vertrieb oder andere Aufgaben für die großen Pharmaunternehmen übernehmen, wie die oben genannten. Eine Reihe kleinerer Unternehmen haben Fast Data Science mit der KOL-Analyse (Analyse wichtiger Meinungsführer) unter Einsatz von NLP beauftragt. Dies kann die Identifizierung prominenter Akademiker auf dem Gebiet, die Analyse veröffentlichter Literatur , Konferenzberichte oder Transkripte von Interviews mit Gesundheitsdienstleistern umfassen. Das Potenzial für KI in Nebenfunktionen der Pharmaindustrie ist enorm.
Oben: Mithilfe von KI-Algorithmen aus der Pharmabranche können die Erkenntnisse wichtiger Meinungsführer (Key Opinion Leaders, KOLs) analysiert werden. Beispielsweise können mithilfe von NLP Muster in großen Mengen von Transkripten oder Dokumenten identifiziert und in verwertbare Statistiken umgewandelt werden, die für quantitative Entscheidungen verwendet werden können.
Ein Auftragsforschungsinstitut (CRO) ist ein Unternehmen, das die Pharmaindustrie unterstützt, beispielsweise durch die Durchführung klinischer Studien. KI kann die Rekrutierung beschleunigen und Rekrutierungskosten sowie Fluktuation vorhersehen. CROs können Daten analysieren, um Trends zu erkennen und Patienten vorzuschlagen, die wahrscheinlich von einer bestimmten Behandlung profitieren. KI kann auch verwendet werden, um Daten aus Berichten über unerwünschte Ereignisse (AERs), klinischen Entwicklungsplänen (CDPs) und anderen Dokumenten zu klinischen Studien zu extrahieren, die ein CRO verarbeiten muss. Wir haben auch an Projekten gearbeitet, bei denen AERs anonymisiert werden mussten, um die DSGVO oder HIPAA einzuhalten (siehe unseren zugehörigen Blogbeitrag zum Trainieren von Modellen für maschinelles Lernen anhand vertraulicher Daten ). KI kann auch für Kostenanalysen verwendet werden, beispielsweise als Regressionsmodell zur Vorhersage der Kosten oder Komplexität der Durchführung einer klinischen Studie.
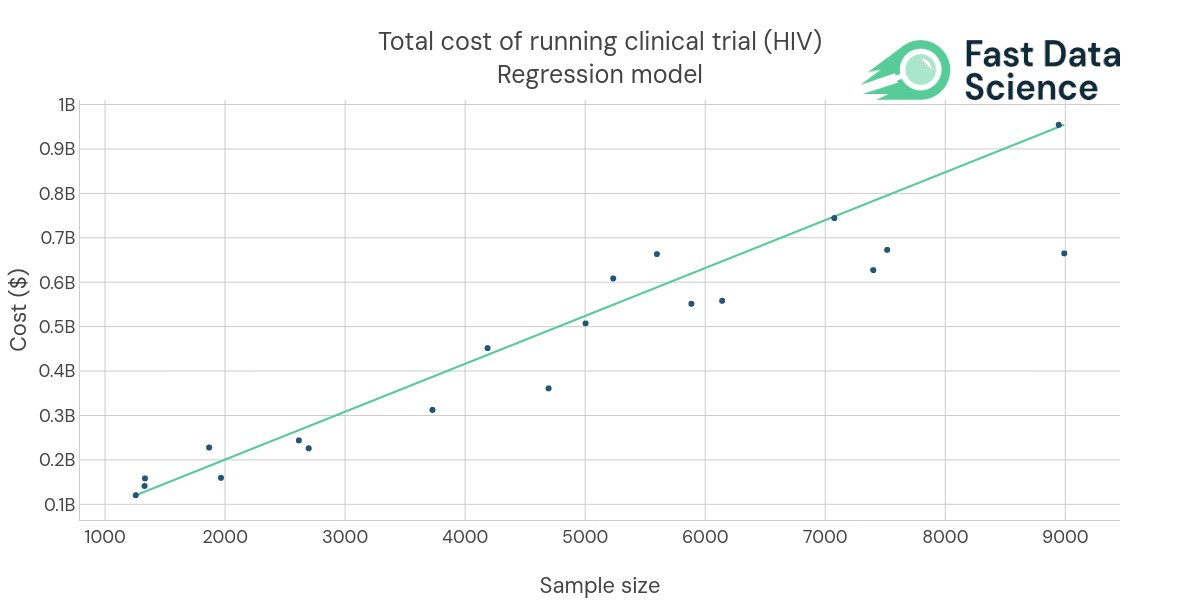
Ein Beispiel aus einem unserer früheren Pharma-KI-Engagements: Wir haben Regressionsmodelle zur Planung der Kosten für die Durchführung klinischer Studien entwickelt. Die oben gezeigten Daten sind aus Gründen der Kundenvertraulichkeit synthetisch.
Weltweit arbeiten zahlreiche vielversprechende Unternehmen an KI in der Pharmaindustrie, von der Arzneimittelentdeckung und präklinischen Entwicklung bis hin zu klinischen und After-Market-Lösungen.
| Pharma-KI-Unternehmen | Standort | Zusammenfassung |
|---|---|---|
| Recursion | USA | Recursion nimmt die In-silico -KI-Vorhersagen von AlphaFold und testet sie experimentell. |
| Google DeepMind | Großbritannien | DeepMind machte erstmals Schlagzeilen, als AlphaGo den weltbesten menschlichen Go-Spieler , den Südkoreaner Lee Sedol, besiegte. Nach AlphaGos Erfolg wandte DeepMinds charismatischer Gründer Demis Hassabis seine Aufmerksamkeit der 3D-Proteinfaltung zu und entwickelte das pharmazeutische KI-Programm AlphaFold , das inzwischen Vorhersagen über die Form von Millionen von Proteinen erstellt hat. |
| Genesis Therapeutics | USA | Genesis Therapeutics hat eine generative KI-Plattform zur Arzneimittelentwicklung entwickelt , die Pharmaunternehmen dabei hilft, neue Medikamente gegen molekulare Ziele zu entdecken, die für Pharmaunternehmen bislang schwer zu erreichen waren. |
| Insilico Medicine | Hongkong | Insilico verwendet Pharma-KI-Modelle, um Zielmoleküle (Proteine, auf die ein Medikament im Körper einwirken soll) und Medikamentenkandidaten für Krankheiten zu identifizieren, wie etwa einen Medikamentenkandidaten mit der vorläufigen Bezeichnung INS018_055, der gegen Lungenfibrose nützlich sein könnte und sich derzeit in Phase 2 der Tests befindet. |
| Insitro | USA | Insitro trainiert Modelle anhand von Gensequenzen, klinischen Ergebnissen und pathologischen Objektträgern. Ihre Modelle können Vorhersagen darüber treffen, wie Krebspatienten wahrscheinlich auf bestimmte Behandlungen reagieren werden. |
| Camino | Großbritannien | Camino verwendet generative KI in der Medizinkommunikation und durchsucht Abstracts und Artikel von PubMed, um Informationen über den Pharmamarkt zu finden, beispielsweise über Wettbewerber um Pharmakunden. |
Es gibt viele mögliche Kombinationen potenzieller Wechselwirkungen zwischen Medikamenten und es ist eine arbeitsintensive Aufgabe, die medizinische Literatur zu lesen, um sie zu identifizieren. Die Gefahr von Nebenwirkungen durch Wechselwirkungen zwischen Medikamenten steigt erheblich, wenn ein Patient mehrere verschreibungspflichtige Medikamente einnimmt.
Deep-Learning- und Text-Mining -Algorithmen wurden bereits eingesetzt, um die wissenschaftliche Literatur zu verarbeiten und mögliche Wechselwirkungen und ihre möglichen Auswirkungen zu identifizieren. Forscher, die Algorithmen für diesen Zweck entwickeln, verwenden die DDIExtraction Challenge als standardisierten Test für Algorithmen, die Wechselwirkungen zwischen Medikamenten identifizieren, und jedes Jahr erreichen neue Deep-Learning -Algorithmen bei dieser Metrik bessere Ergebnisse als je zuvor.
Ein herausfordernder Aspekt der Arzneimittelentwicklung ist die Identifizierung von Zielen für die Arzneimittelentwicklung . Zielmoleküle sind Moleküle im Körper, die mit einer bestimmten Krankheit in Zusammenhang stehen. Wenn das Zielmolekül identifiziert ist, kann nach Kandidatenmolekülen gesucht werden, die wahrscheinlich mit diesem Ziel interagieren und die Krankheit hemmen.
Der Kandidat für ein Medikament gegen Bauchspeicheldrüsenkrebs BPM31510, das Berg mithilfe der Arzneimittelforschung durch künstliche Intelligenz entwickelt hat. Mit diesem Ansatz konnte Berg ein Arzneimittelkandidat namens BPM31510 herstellen, das kürzlich die Phase-2-Studien für Bauchspeicheldrüsenkrebs im fortgeschrittenen Stadium abgeschlossen hat. Die Weiterentwicklung der Verbindung von in silico zu in vitro war ein Vorzeigeerfolg für die künstliche Intelligenz in der Pharmaindustrie.
Das KI-Biopharmaunternehmen Berg hat einen Deep-Learning- Ansatz verwendet, um Wirkstofftargets zu identifizieren. Sie haben eine Reihe von Gewebeproben von Patienten mit und ohne eine bestimmte Krankheit entnommen und das Gewebe einer Reihe von Medikamenten und Bedingungen ausgesetzt. Die Reaktion des Gewebes wird aufgezeichnet und in einen Deep-Learning -Algorithmus eingespeist, der nach möglichen Veränderungen des Krankheitszustands sucht und so zu Kandidatenproteinen führt, die mit der Krankheit in Verbindung stehen könnten. Das Projekt hat das Potenzial der KI in der Pharmaindustrie der Öffentlichkeit zugänglich gemacht.
Wenn potenzielle Medikamente identifiziert wurden, führt das Pharmaunternehmen klinische Studien durch, bevor das Medikament zugelassen werden kann. In Phase-0-Studien werden die Medikamente an einer kleinen Anzahl von Menschen getestet, um zu verstehen, wie sie sich auf den Körper auswirken. In Phase-I-Studien wird das Medikament 15 bis 30 Patienten verabreicht, um mögliche Nebenwirkungen zu verstehen. Anschließend folgen Phase-II-Studien, in denen untersucht wird, ob das Medikament eine Wirkung auf die Krankheit hat, und Phase-III-Studien, an denen mehr als 100 Patienten teilnehmen und die einen Vergleich mit bestehenden Medikamenten beinhalten.
Ab 2020 betragen die durchschnittlichen Kosten für die Markteinführung eines neuen Medikaments 1,3 Milliarden US-Dollar . Und selbst dann schafft es nur ein kleiner Teil der Medikamente aus Phase I bis zur Phase III und Zulassung. Wenn eine klinische Studie durchgeführt wird, muss das Pharmaunternehmen einen detaillierten Plan für die Studie erstellen, in der Regel ein 200-seitiges PDF-Dokument, in dem vertrauliche Informationen geschwärzt sind, und ihn an eine Datenbank wie clinicaltrials.gov übermitteln.
Bei Fast Data Science haben wir ein Convolutional Neural Network entwickelt, um Protokolle für klinische Studien für Boehringer Ingelheim zu verarbeiten und verschiedene Komplexitätsmetriken vorherzusagen, mit denen das Pharmaunternehmen die Kosten für die Durchführung der Studie berechnen kann. Das neuronale Netzwerk kann einen in einfachem Englisch verfassten Bericht eines beliebigen Pharmaunternehmens lesen und eine Reihe quantitativer Metriken in Bezug auf die Komplexität der Studie erstellen. Dies ermöglicht es dem Unternehmen, die Kosten im Voraus abzuschätzen und Studien so zu planen, dass sowohl Kosten als auch Risiken reduziert werden.
Lim et al., Extraktion von Arzneimittelwechselwirkungen aus der Literatur mithilfe eines rekursiven neuronalen Netzwerks , PLoS ONE (2018)
Freedman, Mit KI auf der Suche nach neuen Medikamenten , Scientific American (2020)
Segura-Bedmar et al., Erkenntnisse aus der gemeinsamen Aufgabe DDIExtraction-2013 (2014)
The Economist, Künstliche Intelligenz übernimmt die Arzneimittelentwicklung (2014)
Wouters OJ, McKee M, Luyten J. Geschätzte erforderliche Forschungs- und Entwicklungsinvestitionen, um ein neues Medikament auf den Markt zu bringen , 2009-2018, JAMA. 2020;323(9):844-853. doi:10.1001/jama.2020.1166
What we can do for you